中國新藥研發(fā)助推全球醫(yī)學(xué)科學(xué)新跨越
灣區(qū)時訊(編輯/劉秀 通訊員/文朝陽 陳鋆 趙現(xiàn)廷 )1月6日,,中山大學(xué)腫瘤防治中心徐瑞華教授團(tuán)隊在國際權(quán)威腫瘤學(xué)期刊《柳葉刀腫瘤》(The Lancet Oncology)上公布了一項具有里程碑意義的臨床研究:靶向Claudin 18.2的抗體偶聯(lián)藥物(CMG901)治療晚期胃癌/胃食管結(jié)合部腺癌患者的I期臨床試驗結(jié)果。作為全球首個針對Claudin 18.2靶點的抗體偶聯(lián)藥物臨床研究報道,,國內(nèi)原研的CMG901在晚期胃癌/胃食管結(jié)合部腺癌患者中患者中展現(xiàn)的良好安全性與顯著療效,,標(biāo)志著中國在抗腫瘤新藥研發(fā)領(lǐng)域取得了又一重大突破。

繼化療,、靶向和免疫時代之后,,抗體偶聯(lián)藥物(ADC)開啟了抗腫瘤治療的新篇章,通過將高活性細(xì)胞毒素與抗體結(jié)合,,實現(xiàn)了對腫瘤細(xì)胞的精準(zhǔn)打擊,,同時最大限度地減少了對正常細(xì)胞的影響。全球范圍內(nèi)已有多種ADC藥物獲得批準(zhǔn)上市,,而CMG901(AZD0901)作為一種潛在的全球首創(chuàng),、靶向Claudin 18.2的ADC,通過其獨特的鏈接體與單甲基奧瑞他汀E(MMAE)的結(jié)合,,展現(xiàn)了其在臨床前研究中的卓越效果,。CMG901能夠特異性地與細(xì)胞表面的Claudin18.2結(jié)合,并通過直接細(xì)胞毒性,、抗體依賴性細(xì)胞毒性(ADCC),、補(bǔ)體依賴性細(xì)胞毒性(CDC)以及旁觀者殺傷效應(yīng)來消滅腫瘤細(xì)胞。
徐瑞華教授團(tuán)隊在全球范圍內(nèi)首次發(fā)表靶向Claudin 18.2的ADC藥物的I期臨床研究結(jié)果,,這一成果不僅為CMG901的國際認(rèn)可奠定了堅實基礎(chǔ),,也使其成功授權(quán)給國外知名藥企,并成為全球首批進(jìn)入III期臨床研究的Claudin 18.2ADC藥物,。這一成就不僅是“中國學(xué)者+國產(chǎn)新藥”在抗腫瘤新藥研發(fā)領(lǐng)域的又一突破,,也在中國新藥研發(fā)史上具有里程碑式的意義。
CMG901研究開啟胃癌治療新篇章
胃癌,,這一在全球癌癥中死亡率和發(fā)病率均居高不下的惡性腫瘤,,往往在發(fā)現(xiàn)時已進(jìn)入晚期,其5年總生存率大約只有30%,。Claudin 18.2在胃癌,、食管癌、胰腺癌等多種惡性腫瘤中呈現(xiàn)高特異性表達(dá),,因此成為胃癌靶向治療的理想靶點,。
2020年12月24日至2023年2月23日期間,,研究共納入27例晚期實體瘤患者(其中13例為胃癌/胃食管結(jié)合部腺癌,14例為胰腺癌)進(jìn)行劑量遞增階段的研究,,以及107名晚期胃癌或胃食管連接部癌患者進(jìn)行劑量擴(kuò)展階段的研究,,這些患者均為多線標(biāo)準(zhǔn)治療后失敗的患者。研究分析了2.2 mg/kg,、2.6 mg/kg和3.0 mg/kg三個劑量組胃癌/胃食管結(jié)合部腺癌患者的療效數(shù)據(jù),,在109例病灶可評價患者中,客觀緩解率(ORR)為29%,,經(jīng)確認(rèn)的疾病控制率(DCR)為65%,。其中,89例Claudin 18.2高表達(dá)(定義為≥20%腫瘤細(xì)胞中Claudin 18.2染色強(qiáng)度≥2+)的患者,,經(jīng)確認(rèn)的ORR為35%,,經(jīng)確認(rèn)的DCR為70%。所有Claudin 18.2高表達(dá)患者中,,中位無進(jìn)展生存期(PFS)為4.8個月,,中位總生存期(OS)為11.8個月。研究最終確定CMG901的推薦劑量為2.2 mg/kg,,為后續(xù)III期研究的開展提供了支持,,提示CMG901有望在未來成為Claudin 18.2高表達(dá)胃癌/胃食管結(jié)合部腺癌患者的治療新選擇。
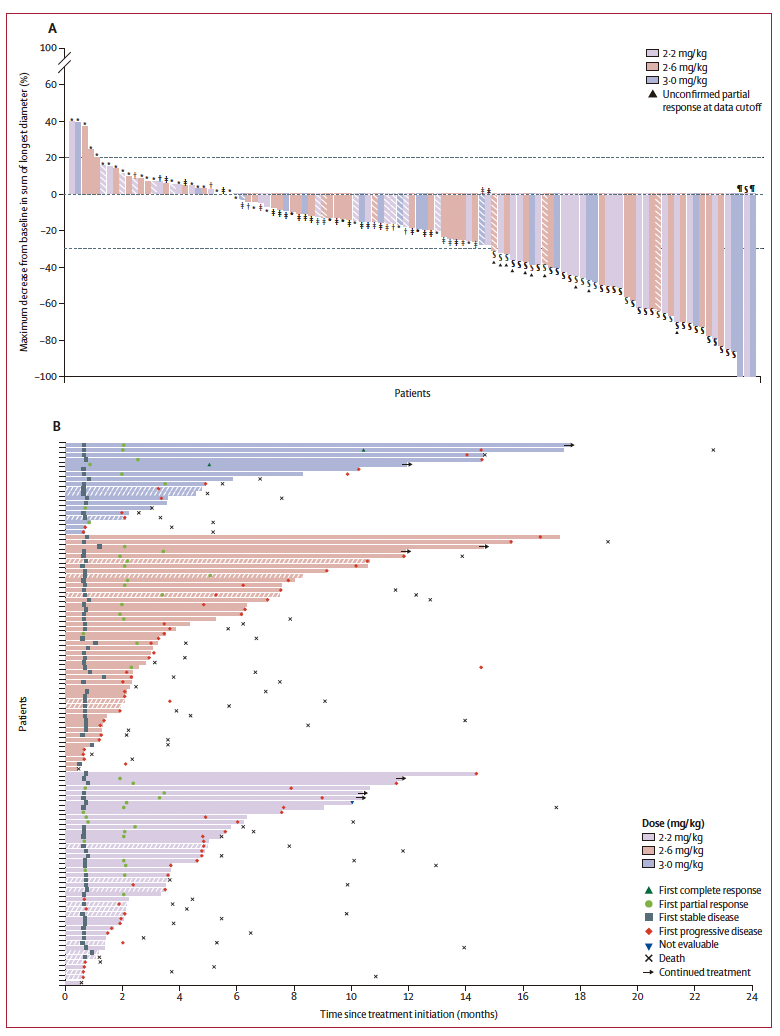
胃癌/胃食管結(jié)合部腺癌(A)最佳總體療效和(B)治療反應(yīng)的持續(xù)時間
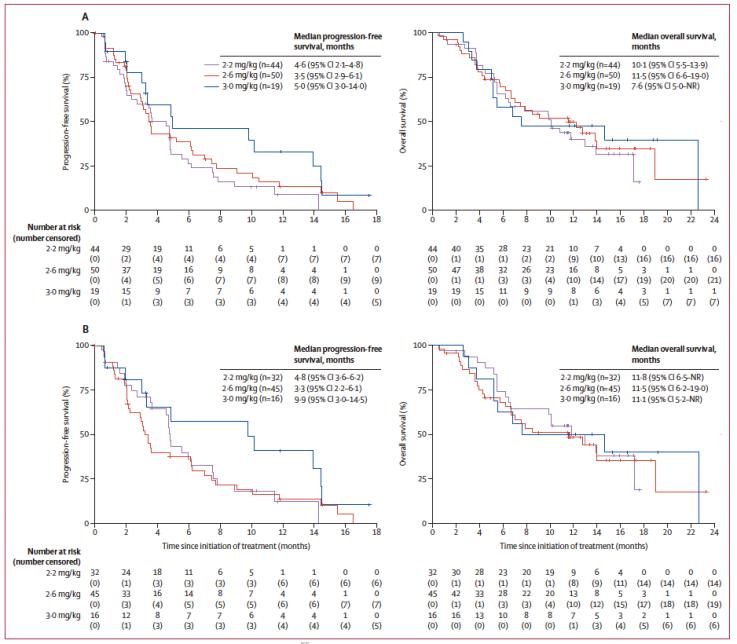
研究中PFS和OS的Kaplan-Meier曲線
(A)胃癌/胃食管結(jié)合部腺癌患者,;(B)Claudin 18.2高表達(dá)胃癌/胃食管結(jié)合部腺癌患者。
在安全性方面,,CMG901同樣表現(xiàn)良好,。在劑量遞增階段,僅2.2 mg/kg組1例患者發(fā)生劑量限制性毒性,,未達(dá)到最大耐受劑量,。在劑量擴(kuò)展階段,雖然68%的患者發(fā)生了≥3級治療期不良事件(TEAEs),,但最常見的≥3級TEAEs是中性粒細(xì)胞計數(shù)降低(21%),、貧血(14%)和嘔吐(10%)。治療相關(guān)的毒性在充分的支持治療中可得到緩解,,患者整體耐受良好,。
中國新藥研發(fā)助推全球醫(yī)學(xué)科學(xué)新跨越
自項目開展以來,CMG901便備受全球關(guān)注,。2023年11月8日,,研究的初步結(jié)果亮相美國腫瘤學(xué)年會全體大會系列會議 (ASCO Plenary Series),作為全球首個抗Claudin 18.2抗體偶聯(lián)藥物臨床研究結(jié)果發(fā)布,,并入選2024 ASCO年會的Education Session (教育專場) 全體會議口頭報告,,得到了國際同行的廣泛關(guān)注和討論,。
值得一提的是,CMG901(AZD0901)目前正在開展國際,、多中心III期研究(NCT06346392),,探索CLDN18.2表達(dá)的晚期實體患者中,CMG901(AZD0901)單藥與研究者選擇標(biāo)準(zhǔn)治療的療效和安全性比較,。臨床研究地點涵蓋美國,、英國、法國,、德國等,,代表了我國自主研發(fā)的Claudin 18.2 抗體偶聯(lián)藥物走出國門,有望在未來獲得歐美國家的適應(yīng)癥批準(zhǔn),,為全球晚期胃癌/胃食管結(jié)合部腺癌患者帶來福音,。
科技創(chuàng)新是發(fā)展新質(zhì)生產(chǎn)力的核心要素。習(xí)近平總書記指出,,“必須加強(qiáng)科技創(chuàng)新特別是原創(chuàng)性,、顛覆性科技創(chuàng)新,加快實現(xiàn)高水平科技自立自強(qiáng),。”在健康領(lǐng)域,,“中國學(xué)者+國產(chǎn)新藥”的研發(fā)模式正成為新質(zhì)生產(chǎn)力蓬勃發(fā)展的鮮明例證。這一模式不僅彰顯了我國科研人員在醫(yī)藥領(lǐng)域的深厚底蘊(yùn)和創(chuàng)新能力,,更體現(xiàn)了我國醫(yī)藥產(chǎn)業(yè)從跟跑,、并跑到領(lǐng)跑的歷史性跨越,通過不懈的努力和持續(xù)的探索,,我們正以前所未有的勇氣和決心,,向著“新”的領(lǐng)域邁進(jìn),以“質(zhì)”取勝,,致力于將更多中國原創(chuàng)藥物推向全球市場,,繼續(xù)為醫(yī)學(xué)科學(xué)貢獻(xiàn)中國智慧和力量。
研究者簡介:

徐瑞華 通訊作者
中國醫(yī)學(xué)科學(xué)院學(xué)術(shù)咨詢委員會學(xué)部委員,,中山大學(xué)腫瘤防治中心主任,、醫(yī)院院長、研究所所長,,教授,,博士生導(dǎo)師,華南惡性腫瘤防治全國重點實驗室主任,。中國臨床腫瘤學(xué)會前任理事長,,中國抗癌協(xié)會副理事長,中國抗癌協(xié)會靶向治療專委會首屆主任委員,中國抗癌協(xié)會化療專委會候任主任委員,,中國臨床腫瘤學(xué)會腸癌專委會主任委員,,以最后通訊作者(少量共同)在NEJM、JAMA(2),、BMJ,、Cell、Nature Med(5),、Nature Mater,、Lancet Oncol(3)、Cancer Cell(3),、Ann Oncol(2),、JCO(2)、Lancet G&H(2),、JAMA Oncol(2)等發(fā)表高水平成果論文200 余篇(35篇IF>30),,成果被寫入57部國際指南,連續(xù)3年入選科睿唯安(Clarivate)全球高被引科學(xué)家,,連續(xù)7年入選中國高被引學(xué)者榜單,,H指數(shù)86。以第一完成人獲國家科技進(jìn)步二等獎2項,、中華醫(yī)學(xué)科技獎,、教育部科技獎及廣東省科技獎等省部級一等獎共7項。全國創(chuàng)新爭先獎1項,、何梁何利基金科學(xué)與技術(shù)進(jìn)步獎,、吳階平醫(yī)藥創(chuàng)新獎、談家楨臨床醫(yī)學(xué)獎及CSCO年度成就獎,。入選國家百千萬人才工程,、全國先進(jìn)工作者、國務(wù)院特殊津貼專家,、南粵百杰人才培養(yǎng)工程、國家衛(wèi)生計生突出貢獻(xiàn)中青年專家等人才項目,。

張東生 通訊作者
中山大學(xué)腫瘤防治中心內(nèi)科五區(qū)區(qū)長,,I期病房II區(qū)區(qū)長(兼),主任醫(yī)師,、醫(yī)學(xué)博士(M.D.,、Ph.D.)。博士研究生導(dǎo)師,,中山大學(xué)腫瘤防治中心中西醫(yī)結(jié)合研究中心副主任,,香港中文大學(xué)Research fellow;Mayo Clinic胃腸癌癥中心訪問學(xué)者,中國初級衛(wèi)生保健基金會消化腫瘤專委會主任委員,,中國抗癌協(xié)會腫瘤藥物臨床研究專業(yè)委員會常委,,廣東省臨床醫(yī)學(xué)會免疫治療專委會副主任委員,廣州市支持與康復(fù)專業(yè)委員會副主任委員,,廣東省抗癌協(xié)會生物治療專業(yè)委員會常委,,廣東省醫(yī)學(xué)會臨床腫瘤內(nèi)科專業(yè)委員會常委,中國抗癌協(xié)會腫瘤化療專業(yè)委員會委員,,廣東省臨床醫(yī)學(xué)會消化腫瘤協(xié)作組組長,。

阮丹云 第一作者
中山大學(xué)腫瘤防治中心臨床研究部一期病房副主任醫(yī)師、醫(yī)學(xué)博士,、碩士生導(dǎo)師,,中華醫(yī)學(xué)會創(chuàng)新藥物治療學(xué)組委員會委員,中國醫(yī)藥教育協(xié)會腫瘤藥物臨床研究專委會委員,,廣東省抗癌協(xié)會大腸癌專業(yè)委員會委員,,廣東省抗癌協(xié)會腫瘤靶向治療專委會青委會常務(wù)委員,廣東省藥學(xué)會腫瘤免疫治療專家委員會委員,。主要從事抗腫瘤新藥臨床研究與腫瘤內(nèi)科治療,,研究方向為I期臨床試驗與轉(zhuǎn)化研究,消化道腫瘤個體化治療,。作為多項抗腫瘤新藥臨床研究項目Key Sub-I,。主持和參與多項國家自然科學(xué)基金及省部級科研基金。
論文鏈接:
https://www.sciencedirect.com/science/article/pii/S1470204524006363
責(zé)任編輯/觀察君











評論 0